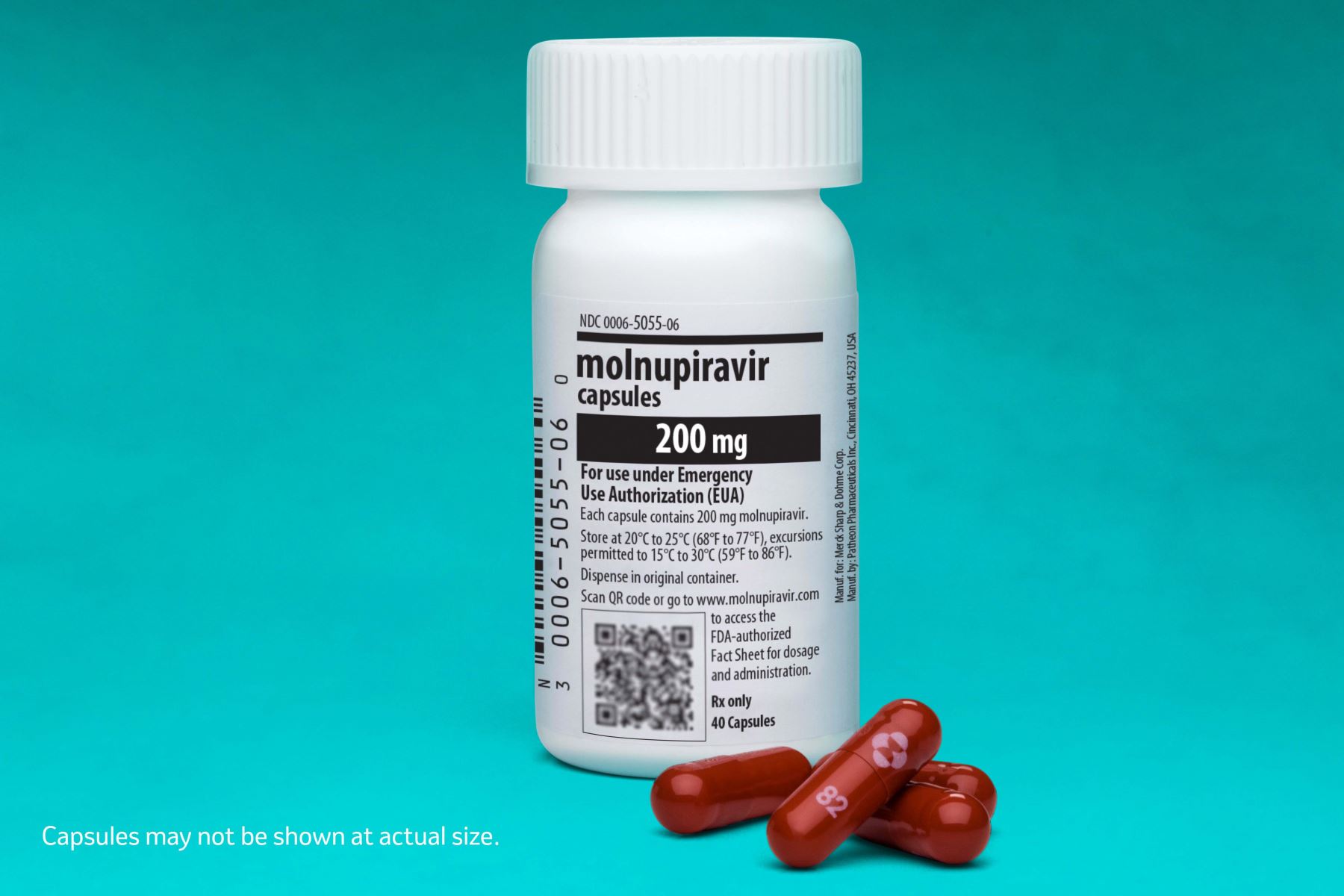
La Dirección General de Medicamentos, Insumos y Drogas (Digemid) otorgó este jueves el Registro Sanitario Condicional al Molnupiravir, píldora para el tratamiento contra el covid-19, a fin de permitir su comercialización en el país con receta médica.
El fármaco ha sido desarrollado por la farmacéutica Merck Sharp & Dohme (MSD), la cual asegura que la píldora ha demostrado eficacia y seguridad en la reducción de hospitalizaciones y muertes por coronavirus.
El Ministerio de Salud (Minsa), aclaró que no ha sido adquirido por la entidad para ser usado como tratamiento.
«El Minsa aclara que el fármaco Molnupiravir usado como tratamiento para la COVID-19 ha recibido un registro sanitario emitido por Digemid, pero no ha sido adquirido por el Ministerio de Salud para brindar tratamiento».
¿Qué es el Molnupiravir?
El molnupiravir, cuyo uso para tratar la COVID-19, es un antiviral que inhibe la replicación del SARS-CoV-2 y que se usa los primeros cinco días de detectado el virus en algunos pacientes adultos.
Este medicamento ya ha sido aprobado en varios países como Estados Unidos, Japón, India y México, se prescribe a pacientes adultos que se encuentran dentro de los primeros cinco días desde el inicio de los síntomas de la enfermedad y que presentan al menos un factor de riesgo para desarrollar complicaciones graves.
¿Quiénes pueden tomar Molnupiravir?
La píldora se prescribe a los adultos que están dentro de los primeros 5 días desde el inicio de los síntomas y que presenten, al menos, un factor de riesgo para desarrollar la enfermedad grave.
Alberto La Rosa, el gerente médico en Perú de la farmacéutica Merck Sharp & Dohme, informó en Canal N, que esta pastilla contra el COVID-19 no es de uso masivo, sino que está dirigida a quienes más podría afectar el virus: personas con comorbilidades y adultos mayores.
Con información de Andina e Infobae
Síguenos en nuestras redes sociales:
- Facebook: Diario El Tiempo
- Twitter: @eltiempopiura
- Instagram: @eltiempopiura
- YouTube: Diario El Tiempo
- TikTok: @eltiempopiura